体外診断用医薬品の製造販売承認の種類のひとつに「緊急承認」というものがあります。
緊急承認では、有効性が推定された段階で承認がおこなわれることから、承認後2年間という期限が設定されます。
承認を受けた製造販売業者は、この2年間の期限内に有効性の確認をおこない、再度承認申請をしなければなりません。
では、緊急承認の2年間の期限は延長することが可能なのでしょうか?
結論から言うと、緊急承認の期限は1年を超えない範囲内において延長することができます。
本ページでは、緊急承認の期限の延長について根拠法令とともに解説します。
医薬品医療機器等法
根拠条文
さっそくですが、まずは関連する法律の条文をご紹介します。
緊急承認の期限の延長に関する規定は医薬品医療機器等法の<第23条の2の6の2第3項>に書かれています。
こちらが根拠となる条文になります。
<第23条の2の6の2第3項>
厚生労働大臣は、第5項の申請に係る第23条の2の5第2項第3号の規定による審査を適正に行うため特に必要があると認めるときは、薬事審議会の意見を聴いて、第1項の期限を1年を超えない範囲内において延長することができる。
令和5年法律第36号による改正後の医薬品医療機器等法(2024年4月1日施行)
原文は 総務省 e-Gov法令検索 でご確認いただけます。
簡単に解釈すると、
- 適正に承認審査をおこなうために必要があるときには緊急承認の期限を延長するよ~
- 期限の延長は1年以内としますよ~
という感じのことが書かれています。
図に起こしてみましょう。
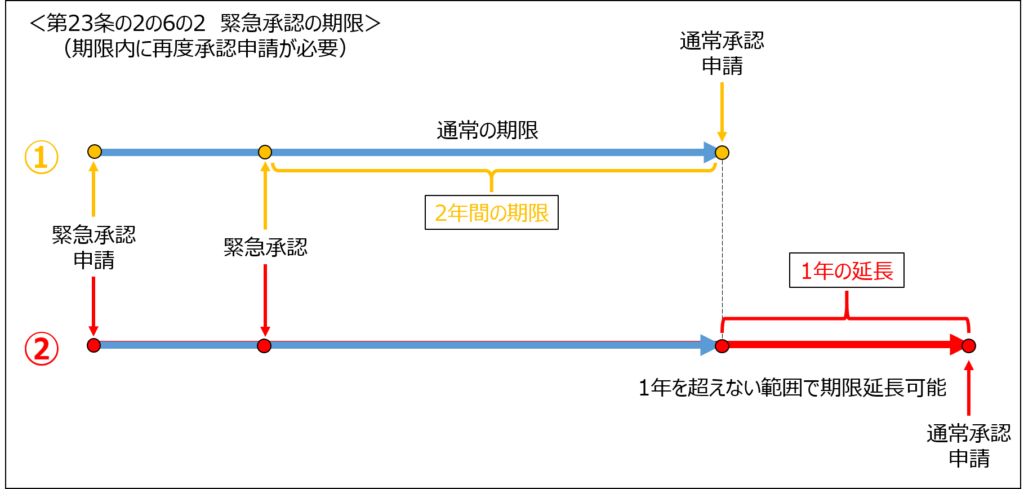
通常だと、①のように緊急承認の期限は原則2年間となっていますが、
適正な承認審査のために必要があるとされた場合には、②のように期限は最大で1年間延長されます。
なんとなく理解できたでしょうか?
詳しく見ていきましょう。
厚生労働大臣が期限を延長する
この条文の主語は「厚生労働大臣」となっています。
そのため、厚生労働大臣の権限で期限が延長されます。
「もうちょっと販売利益を得たいなぁ」といった企業(製造販売業者)都合で延長できるわけではありませんので注意が必要です。
あくまで、厚生労働大臣が適正な審査のために必要と認めたときにのみ延長されるというものです。
とはいえ、厚生労働大臣の独断により延長されるものでもありません。
延長に際しては、「薬事審議会」の意見を聴くことになります。
審査を適正に行うため特に必要があると認めるとき
期限の延長については「審査を適正に行うため特に必要があると認めるとき」に適用されます。
「審査を適正に行うため特に必要があると認めるとき」に該当するかどうかについては詳細な基準は示されていませんが、例えば次のものを総合的に勘案して決定されるようです。
- 有効性を確認するために必要な資料の提出の時期
- 猶予資料の提出の時期
- 承認後の各種調査の実施に係る時期
- 緊急承認において措置された表示等に係る特例が不要となる時期
有効性を確認するための使用成績調査等に時間がかかると予測されるようであれば、おのずと期限は長めに設定されることになると、思われます。
1年を超えない範囲内
期限の延長は、「1年を超えない範囲内」において実施されます。
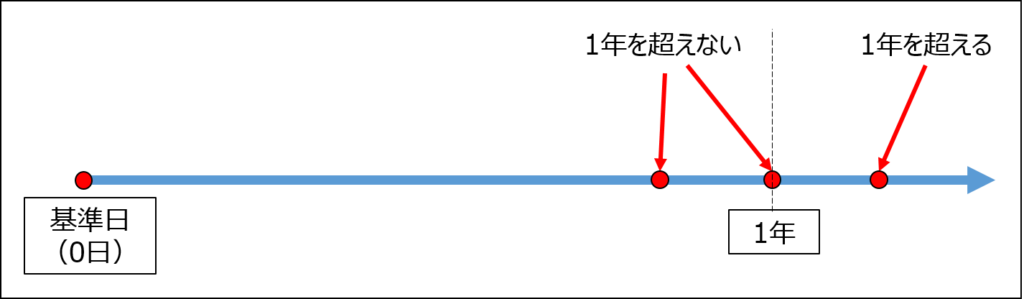
「1年を超えない範囲内」ですので、「ちょうど1年」が最長となります。
具体例を見てみましょう。
もともとの承認の期限が2024年5月20日の場合、
1年を超えない範囲内、つまり、最長で2025年5月20日まで延長することができます。
他の製品の緊急承認の期限
緊急承認の制度は体外診断用医薬品以外にも、医薬品、医療機器、再生医療等製品にも適用されます。
これらの製品の期限も見ていきましょう。
| 種類 | 延長規定 | 根拠条文(法律) | |
|---|---|---|---|
| 医薬品 | 1年を超えない範囲 | 厚生労働大臣は、第5項の申請に係る第14条第2項第3号の規定による審査を適正に行うため特に必要があると認めるときは、薬事・食品衛生審議会の意見を聴いて、第1項の期限を1年を超えない範囲内において延長することができる。(法第14条の2の2第3項) | |
| 医療機器 | 1年を超えない範囲 | 厚生労働大臣は、第5項の申請に係る第23条の2の5第2項第3号の規定による審査を適正に行うため特に必要があると認めるときは、薬事・食品衛生審議会の意見を聴いて、第1項の期限を1年を超えない範囲内において延長することができる。(法第23条の2の6の2第3項) | |
| 再生医療等製品 | 1年を超えない範囲 | 厚生労働大臣は、第五項の申請に係る第二十三条の二十五第二項第三号の規定による審査を適正に行うため特に必要があると認めるときは、薬事・食品衛生審議会の意見を聴いて、次条第一項の期限を、1年を超えない範囲内において延長することができる。(法第23条の26の2第3項の規定により準用する法第23条の26第2項) |
表1. 体外診断用医薬品以外の製品の緊急承認の期限
全て「1年を超えない範囲内」で延長が可能となっています。
体外診断用医薬品と同じですね。
まとめ
本ページでは緊急承認の期限について、その根拠を実際の法令を見ながら確認しました。
体外診断用医薬品の緊急承認の期限は原則2年となっていますが、
「審査を適正に行うため特に必要があると認めるとき」には「厚生労働大臣」によって「1年を超えない範囲内」で期限が延長されることがあります。

緊急承認の対象となる体外診断用医薬品はまだありませんけどもねー。
以上です!ありがとうございました!

コメント